Nya kunskaper om vikten av kurativ behandling vid njurcancer
Varje år diagnostiseras cirka 1 300 nya fall av njurcancer i Sverige.

2022-02-07
Hur ser biverkningsprofilen ut för KEYTRUDA® (pembrolizumab) i kombination med kemoterapi? Och vad finns det för rekommendationer för hantering av immunrelaterade biverkningar?
KEYTRUDA® (pembrolizumab), i kombination med kemoterapi, är indikerat som första linjens behandling av metastaserad skivepitel- och icke-skivepitel- icke-småcellig lungcancer (NSCLC) hos vuxna.4 KEYTRUDA® som administreras som monoterapi eller i kombination med kemoterapi har visats ge en överlevnadsvinst* jämfört med enbart kemoterapi.1-3
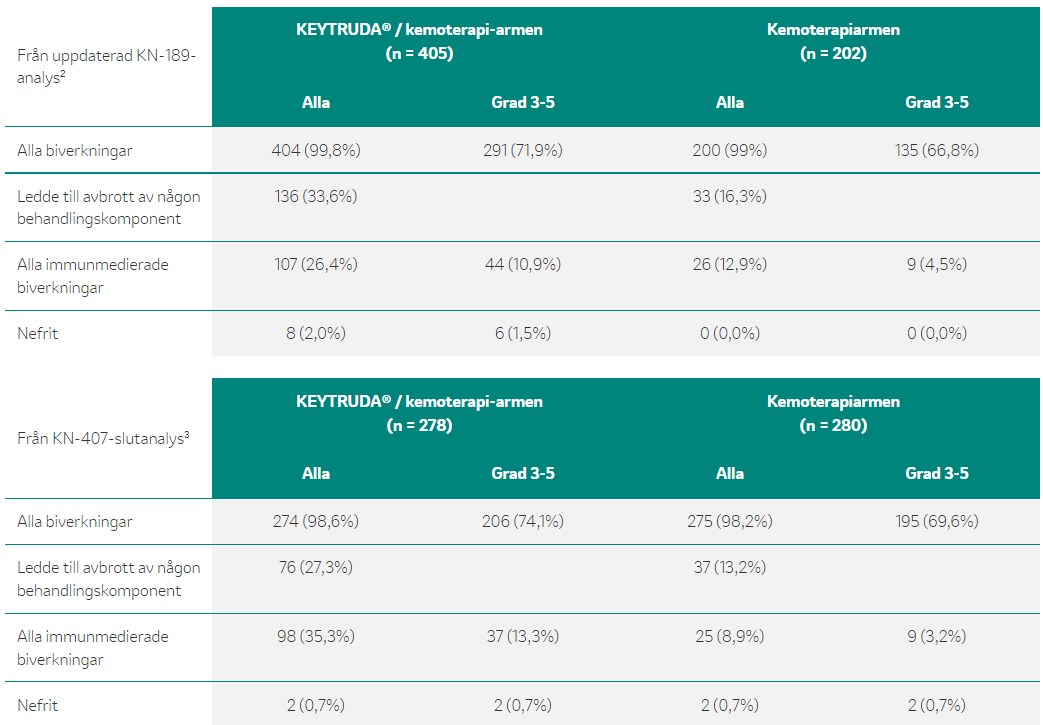
Studier har visat att KETYRUDA® med kemoterapi inte visade förändrad biverkningsprofil mot vad som tidigare rapporterats.2,3
Platinabaserad kemoterapi har länge varit standardbehandling för patienter med metastaserad NSCLC som saknar behandlingsbara mutationer.2 Upptäckten av immuncheckpointhämmare är ett viktigt framsteg inom cancerbehandling som gjorts under det senaste årtiondet.5 Den fortsatta expansionen av immunterapibehandling har lett till ett paradigmskifte i behandlingen av NSCLC och förbättrat patientprognosen.6 En av nackdelarna med dessa framsteg är nya immunrelaterade biverkningar, som skiljer sig från kemoterapirelaterade biverkningar.5 Sjukvårdspersonal har lärt sig att hantera olika immunrelaterade biverkningar, av vilka de vanligaste är gastrointestinala, respiratoriska, endokrina eller dermatologiska. Det finns andra immunrelaterede biverkningar som är sällsynta men som kan vara mycket allvarliga, t.o.m. dödliga, såsom neurologiska rubbningar eller hjärtmuskelinflammation.7 Det är viktigt att identifiera dessa tidigt eftersom de flesta immunrelaterade biverkningar kan hävas, och i många fall kan patienter fortsätta med immunterapibehandlingen, om de immunrelaterade biverkningarna hanteras på rätt sätt.7
ESMO-riktlinjerna för hantering av biverkningar från immunterapi innehåller en översikt över de huvudsakliga immunrelaterade biverkningarna och rekommendationer för hur de ska hanteras.8
Fas 3-studien, KEYNOTE-024, har fastställt KEYTRUDA® monoterapi som ett första linjens behandlingsalternativ för patienter med PD-L1-positiv (TPS ≥ 50 %), metastaserad NSCLC och som saknar mutationer i EGFR eller ALK.9 Resultaten från slutanalysen är i faktaruta 6.
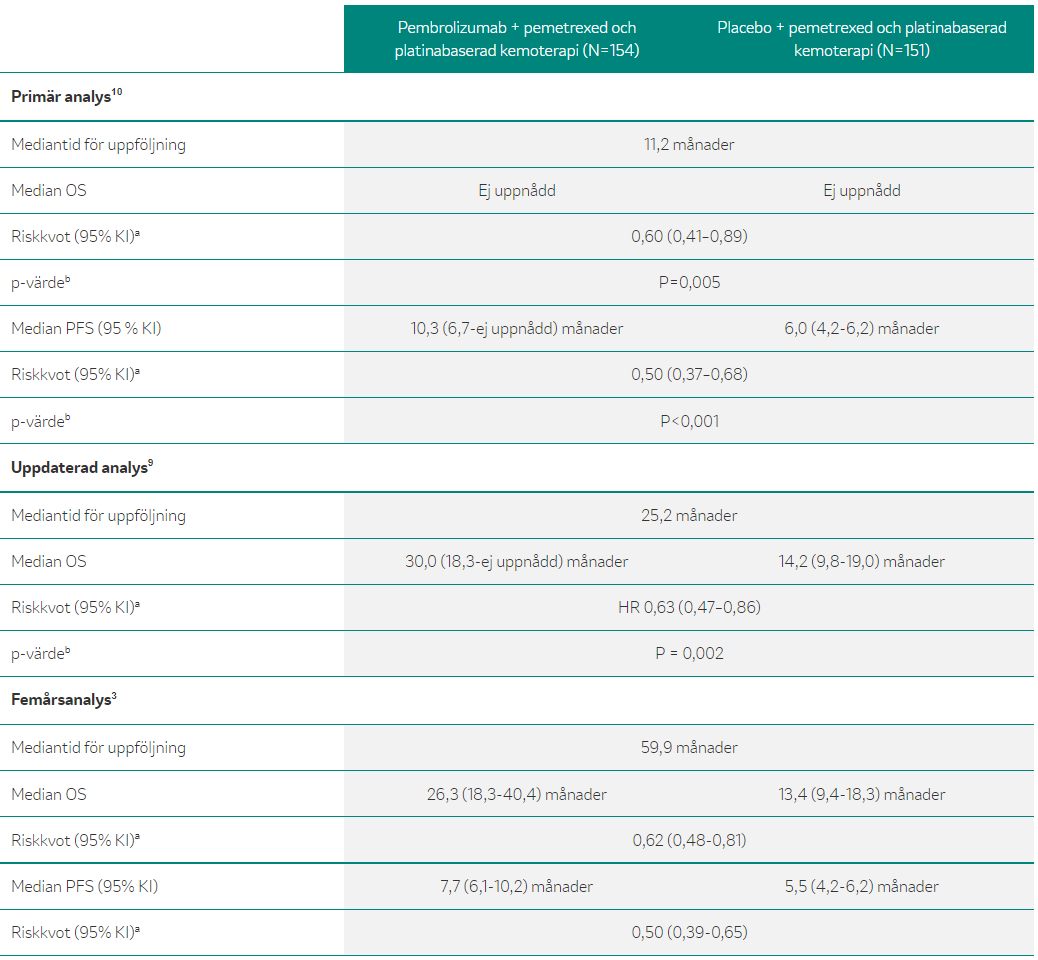
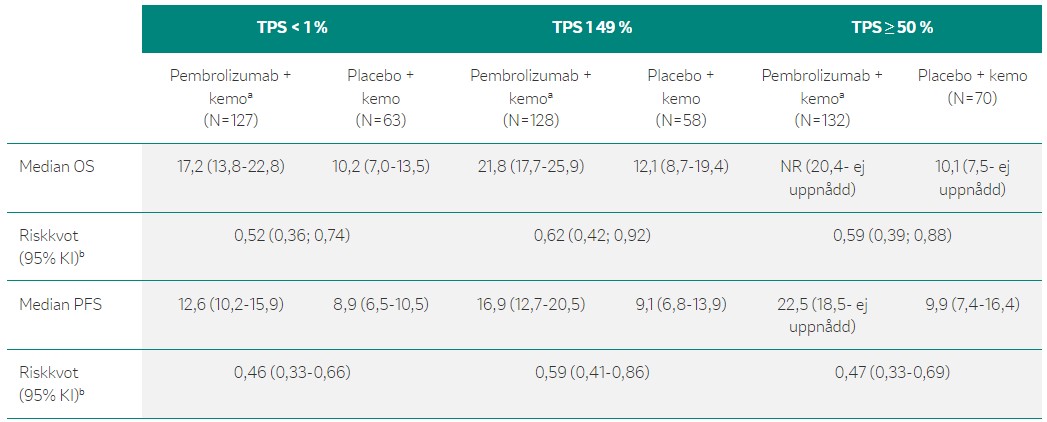
Slutdata från fas 3-studien KEYNOTE-189 på patienter med metastaserad NSCLC av icke-skivepiteltyp visade på signifikant överlevnadsvinst (OS) och progressionsfri överlevnad (PFS) för KEYTRUDA® i kombination med pemetrexed plus cisplatin eller karboplatin (behandlingsarm, N= 410) jämfört med placebo och samma kemoterapiregim (placeboarm, N=206). Med en medianuppföljningstid på 18,8 månader var risken för död signifikant reducerad med 44 % i behandlingsarmen, och man såg en median-OS på 22,0 vs 10,6 månader [HR = 0,56; p<0,00001] vid jämförelse med placeboarmen. Dessutom var risken för sjukdomsprogression signifikant reducerad med 51 % i behandlingsarmen, jämfört med placeboarmen [HR = 0,49; p<0,00001].4 Resultaten från slutanalysen är i faktaruta 7.
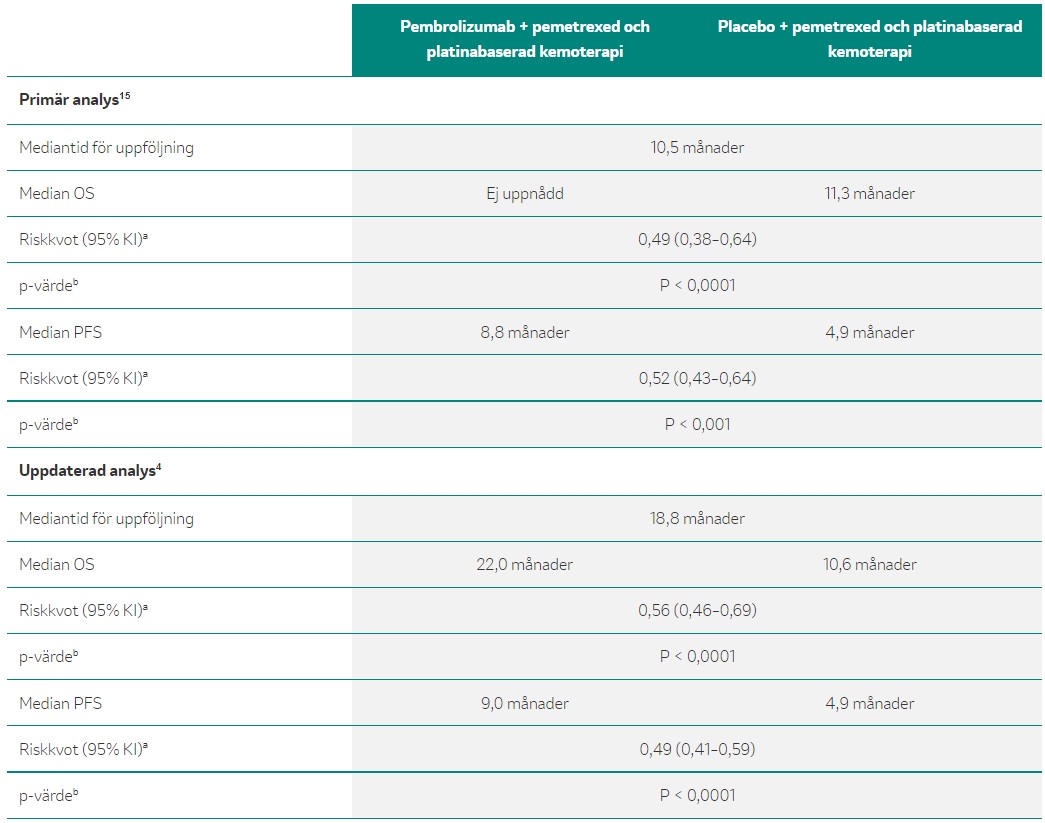
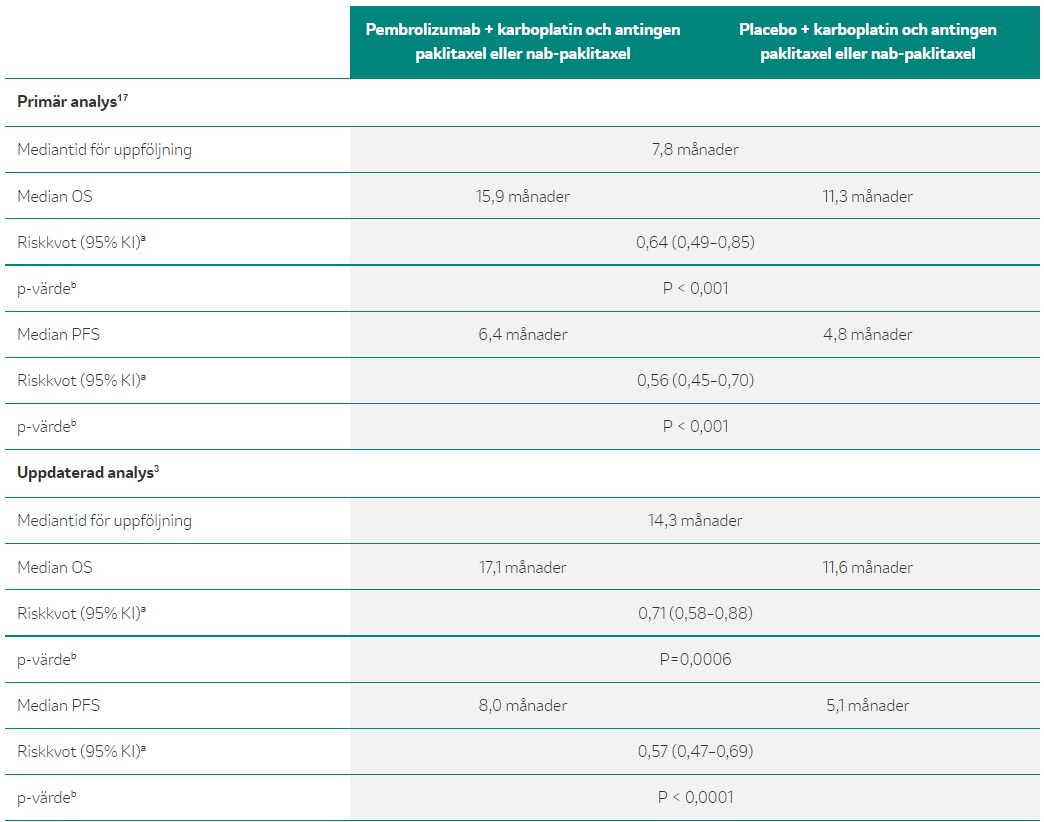
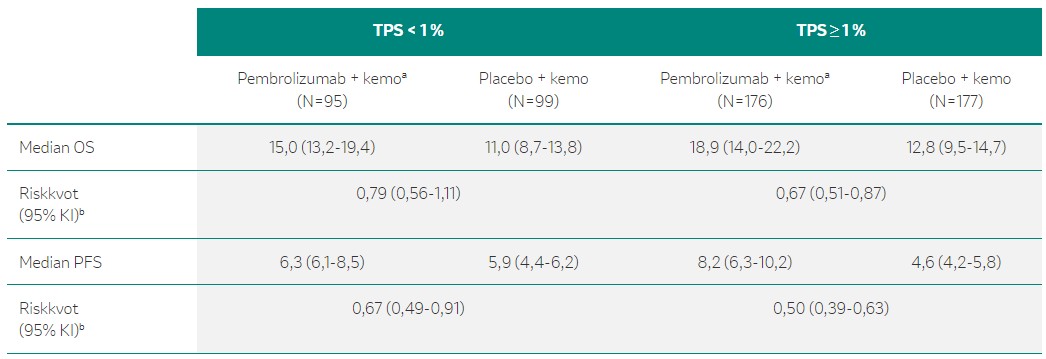
Dessutom visade fas 3-studien, KEYNOTE-407, en signifikant överlevnadsvinst [HR = 0,71; p=0,0006] och progressionsfri överlevnad [HR = 0,57, p<0,0001] med KEYTRUDA® plus karboplatin och paclitaxel eller nab-paclitaxel (N=278) jämfört med placebo plus kemoterapi (N=281) hos patienter med metastaserad skivepitel-NSCLC.4 Resultaten från slutanalysen är i faktaruta 9.
Det är värt att notera att OS och PFS var förbättrad i KEYTRUDA®-armen jämfört med kemoterapi-armen, inte enbart i den totala populationen utan också i de undergrupper som definierades beroende på PD-L1-uttryck.4 Resultaten är i faktaruta 8 och faktaruta 10.
Till följd av dessa resultat är KEYTRUDA® plus platinabaserad kemoterapi nu ett första linjens standardbehandlingsalternativ för patienter med metastaserad NSCLC med lågt eller inget PD-L1-uttryck (TPS<50 %) och som saknar EGFR eller ALK-mutationer.9
Fas 3-studierna har visat att KETYRUDA® med kemoterapi inte visade förändrad biverkningsprofil mot vad som tidigare rapporterats.2,3 Ingen statistisk analys har utförts för jämförelsen av biverkningsprofilen.
När det gäller säkerhetsprofilen för fas 3-studien KEYNOTE-189 har liknande andelar patienter upplevt biverkningar med KEYTRUDA®-kemoterapi som med placebo-kemoterapi: Biverkningar av alla orsaker av grad 3-5 uppträdde hos 71,9 % respektive 66,8 % i KEYTRUDA® plus kemoterapi- respektive placebo plus kemoterapigruppen. Immunrelaterade biverkningar förekom som väntat oftare hos patienter som behandlades med KEYTRUDA® plus kemoterapi (26,4 %, grad 3-5: 10,9 %) jämfört med de patienter som behandlades med placebo plus kemoterapi (12,9 %, grad 3-5: 4,5 %). De vanligaste immunrelaterade biverkningarna hos patienter som behandlades med KEYTRUDA® plus kemoterapi var hypotyreos (7,9 %), hypertyreos (4,9 %) och pneumonit (4,9 %). De biverkningar som förekom under studien överensstämde med dem som är associerade med behandlingens enskilda komponenter, och det fanns ingen evidens för nya biverkningar eller fördröjda biverkningar enligt ytterligare uppföljning.2
Liknande resultat rapporterades i KEYNOTE-407. Biverkningar av alla orsaker av grad 3-5 förekom hos 74,1 % respektive 69,9% i KEYTRUDA® plus kemoterapi- respektive placebo plus kemoterapigruppen. Immunrelaterade biverkningar förekom hos 35,3 % (grad 3-5: 13,3 %) och 8,9 % (grad 3-5: 3,2 %) av de patienter som behandlades med KEYTRUDA® plus kemoterapi respektive placebo plus kemoterapi. De vanligaste immunrelaterade biverkningarna hos patienter som behandlades med KEYTRUDA® plus kemoterapi var de samma som i KEYNOTE-189: Hypotyreos (12,2 %), hypertyreos (6,8 %) och pneumonit (8,3 %).3
Resultaten från KEYNOTE-189 och KEYNOTE-407 visade att behandling av patienter med metastaserad NSCLC med en kombination av KEYTRUDA® och kemoterapi inte visade förändrad biverkningsprofil mot vad som tidigare rapporterats. De förbättrade effektivitetsmåtten (OS och PFS) i de två studierna uppnåddes med hanterbar biverkningsprofil.
* Ingen statistisk analys har utförts för jämförelsen av biverkningsprofilen.
KEYTRUDA som monoterapi är indicerat för behandling av vuxna patienter med:
KEYTRUDA som kombinationsbehandling är indicerat för vuxna patienter med:
KEYNOTE-010-studien, som jämför KEYTRUDA® med docetaxel i cisplatin-refraktorisk NSCLC, visade att behandlingsrelaterade biverkningar av grad 3-5 var mindre vanliga i KEYTRUDA®-grupperna (13 % och 16 %) än i docetaxel-gruppen (35 %).10
KEYNOTE-024-studien, som jämför första linjes KEYTRUDA® med cisplatin-baserad kemoterapi i NSCLC, visade att behandlingsrelaterade biverkningar av grad 3-5 var mindre vanliga i KEYTRUDA®-gruppen (26,6 %) än i kemoterapi-gruppen (53,3 %).11
ESMO-riktlinjerna för hantering av toxiciteter orsakade av immunterapi som publicerades 2017 ger tydliga rekommendationer för hanteringen av irAE beroende på grad:
irAE av grad 1-2
Konservativ eller understödjande behandling rekommenderas. Detta kan innefatta lokala (för hudrelaterade toxiciteter) eller perorala behandlingar för specifika biverkningar.
irAE av grad 3-4
Kräver omedelbar utredning och lämplig åtgärd, vanligen tillfälligt utsättning av immuncheckpointhämmaren tills en lägre svårighetsgrad har nåtts. I vissa fall krävs permanent utsättning.
Anpassat från Haanen JBAG et al., 20178
Det finns även svenska dokument tillgängliga med tydliga rekommendationer för hanteringen av irAE beroende på grad. Till exempel:
Till vänster: Cancercentrum Norr. 2017. Bedömning och hantering av biverkningar. Umeå.12
Till höger: Akademiska sjukhuset 2018. Bedömning och hantering av biverkningar i samband med immunterapi med checkpointhämmare.13


Det finns ännu inga kliniskt validerade biomarkörer som gör det möjligt med individuellt anpassade bedömningar av risken för irAE. Flera potentiella riskfaktorer har dock identifierats. Dessa potentiella riskfaktorer kan fungera som vägledning för behandlingsbeslut:
Bindvävssjukdom
Vaskulit
Andra autoimmuna sjukdomar
Kombination av immuncheckpointhämmare
Endogena faktorer*
Hög risk för irAE
* Skillnader mellan tumörer och genetiska skillnader, cancerform, tumörmikromiljö och mikrobiota.
Anpassat från Martins F et al., 2019.5
Behandling med pembrolizumab som monoterapi (2 mg/kg kroppsvikt (n=344) eller 10 mg/kg kroppsvikt (n=346))* gav en förbättring av OS och PFS jämfört med docetaxel hos tidigare behandlade patienter med metastaserad NSCLC och PD -L1-uttryck, TPS ≥ 1 %.4
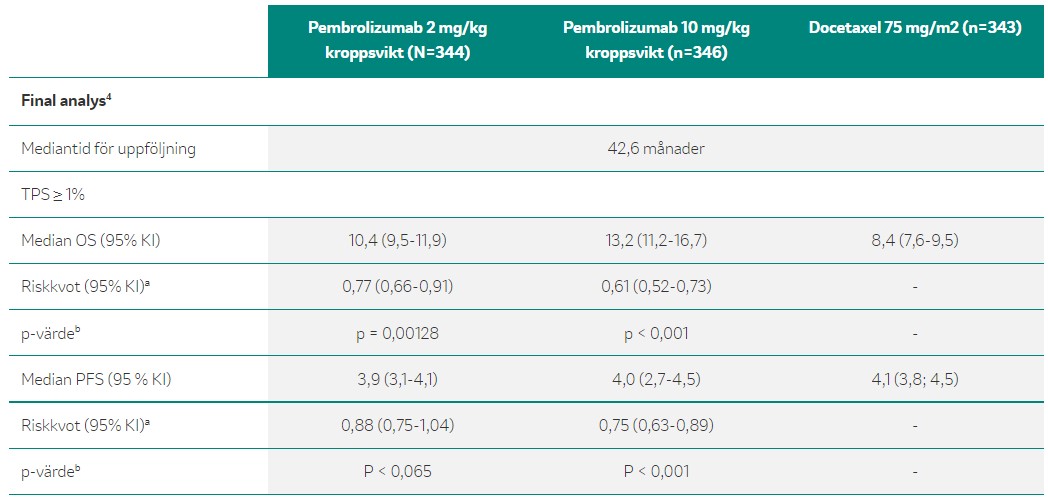
a Hazard ratio (pembrolizumab jämfört med docetaxel) baserat på stratifierad Cox proportional hazard model
b Baserat på stratifierat log-rank test
Anpassat från KEYTRUDA® SPC 01/20224
*Doseringen är inte godkänd
Behandling i första linjen med pembrolizumab i monoterapi gav en signifikant förbättring av OS och PFS jämfört med kemoterapi hos patienter med tidigare obehandlad, metastaserad NSCLC och högt PD -L1-uttryck (TPS ≥ 50 %).14
aHazard ratio (pembrolizumab jämfört med ipilimumab) baserat på stratifierad Cox proportional hazard model bBaserat på stratifierat log-rank test
Anpassat från Reck M. et al. 20164, Reck M. et al. 20199 och Brahmer et al. 20203
Behandling i första linjen med KEYTRUDA® (pembrolizumab) plus pemetrexed och platinabaserad kemoterapi gav en signifikant förbättring av OS och PFS jämfört med placebo plus pemetrexed och platinabaserad kemoterapi hos patienter med metastaserad icke-skivepitel NSCLC, oberoende av PD-L1-uttryck. Viktigt i sammanhanget är att pembrolizumab behandlade patienter hade en mer än dubbelt så hög ORR (48,0 %, 95 % KI 43,1-53,0) som patienter som fick placebo-kemoterapi (19,4 %, 95 % KI 14,2-25,5).2
a Baserat på stratifierad Cox proportional hazard model
b Baserat på stratifierat log-rank test
Anpassat från Gadgeel S. et al. 20202 Gandhi L. et al. 201815 och SPC 01/20224
a Kemo = pemetrexed och platinabaserad kemoterapi
b Hazard ratio (pembrolizumab + kemoterapi jämfört med kemoterapi) baserat på stratifierad Cox proportional hazard model
Anpasset från Gadgeel S. et al. 20202
Behandling i första linjen med pembrolizumab plus karboplatin och antingen paklitaxel eller nab-paklitaxel gav en signifikant förbättring av OS och PFS jämfört med placebo plus karboplatin och antingen paklitaxel eller nab-paklitaxel hos patienter med metastaserad skivepitel-NSCLC, oberoende av PD-L1-uttryck.3
a Baserat på stratifierad Cox proportional hazard model b Baserat på stratifierat log-rank test
Anpassat från Paz-Ares L et al. 20203 och Paz-Ares et al., 201816
a Kemo = pemetrexed och platinabaserad kemoterapi
b Hazard ratio (pembrolizumab + kemoterapi jämfört med kemoterapi) baserat på stratifierad Cox proportional hazard model
Anpasset från Paz-Ares L. et al. 20203
Studie: En randomiserad, öppen, kontrollerad, fas 3-prövning, multicenter. Population: 305 behandlingsnaiva, vuxna patienter med metastatisk icke-småcellig lungcancer och PD-L1-uttryck med TPS ≥50 %. Intervention och komparator: I förhållandet 1:1 fick patienterna pembrolizumab 200 mg var 3:e vecka (n=154) eller platinabaserad kemoterapi (däribland pemetrexed+karboplatin, pemetrexed+cisplatin, gemcitabin+cisplatin, gemcitabin+karboplatin eller paklitaxel+karboplatin) (n=151). Behandlingstid: Maximalt 24 månader eller till sjukdomsprogression eller oacceptabel toxicitet. Primärt effektmått:ektmått: Progressionsfri överlevnad (PFS).
Studie: En uppdaterad analys från KEYNOTE-189: En dubbelblind, randomiserad fas 3-prövning. Population: 616 patienter med metastaserad icke-skivepitel NSCLC utan sensitiserande EGFR- eller ALK-mutationer som inte hade fått någon tidigare behandling för metastaserad sjukdom randomiserades i förhållandet 2:1. Byte till pembrolizumab var tillåten för patienter i placebo-kombinationsgruppen som visade sjukdomsprogression. Interventions- och behandlingstid: Patienterna randomiserades (2:1) till att få pemetrexed och platina plus pembrolizumab (n = 410) eller placebo (n = 206) var 3:e vecka i 4 cykler och fick därefter underhållsbehandling med pemetrexed plus pembrolizumab eller placebo i upp till sammanlagt 35 cykler. Primärt effektmått: De primära effektmåtten var totalöverlevnad (OS) och progressionsfri överlevnad (PFS) bedömt enligt en central blindad, oberoende radiologisk granskning.
Studie: En randomiserad, dubbelblind fas 3-prövning. Randomiseringen stratifierades efter TPS (tumour proportion score) för PD-L1 (≥ 1 % jämfört med < 1 %, där TPS är den procentandel tumörceller som visar PD-L1-färgning av membranet och < 1 % betraktas som PD-L1-negativ), valet av taxan (paklitaxel jämfört med nab-paklitaxel) och geografisk rekryteringsregion. Population: 559 patienter med obehandlad, metastaserad skivepitel-NSCLC. Intervention: I förhållandet 1:1 fick patienterna 200 mg pembrolizumab eller placebo i form av koksaltlösning i upp till 35 cykler. Alla patienter fick dessutom karboplatin och antingen paklitaxel eller nab-paklitaxel (paklitaxel bundet till nanopartiklar av albumin) under de första 4 cyklerna. Behandlingstid: Alla behandlingar gavs intravenöst i 3-veckorscykler. Den tilldelade behandlingen fortsatte till radiografisk sjukdomsprogression, uppträdande av oacceptabla toxiska effekter, en prövares beslut att avbryta behandlingen eller att patienten återkallade sitt samtycke. Primärt effektmått: De primära effektmåtten var totalöverlevnad (OS) och progressionsfri överlevnad (PFS).
*KEYNOTE-189 (median uppföljningstid 18,8 månader): Median (95 % KI) OS vid metastaserad icke-skivepitel NSCLC för KEYTRUDA® i kombination med platinabaserad kemoterapi med pemetrexed (N=410) vs placebo i kombination med platinabaserad och pemetrexed kemoterapi (N=206): 22 (19,5-24,5) månader vs 10,6 (8,7-13,6) månader, HR 0,56; P>0,00001. Median (95 % KI) PFS: 9,0 (8,1-10,4) månader vs 4,9 (4,7-5,5) månader, HR 0,49; p<0,00001. KEYNOTE-407 (median uppföljningstid 14,3 månader): Median (95 % KI) OS vid metastaserad skivepitel icke-småcellig lungcancer (NSCLC) för KEYTRUDA® i kombination med platinabaserad kemoterapi (N=278) vs placebo plus platinabaserad kemoterapi (N=281): 17,1 (14,4-19,9) månader vs 11,6 (10,1-13,7) månader, HR 0,71; p=0,0006. Median (95% KI) PFS: 8,0 (6,3-8,4) månader vs 5,1 (4,3-6,0) månader, HR 0,57; P<0,0001. KEYNOTE-024 (median uppföljningstid 25 månader): Median (95 % KI) OS vid avancerad icke-småcellig lungcancer och PD‑L1-uttryck TPS ≥ 50 % för KEYTRUDA® (N=154) vs platinabaserad kemoterapi (N=151): 30,0 (18,3- ej uppnådd) månader vs 14,2 (9,8-19,0) månader, HR 0,63; P=0,002. Median (95% KI) PFS: 10,3 (6,7- ej uppnådd) månader vs 6,0 (4,2-6,2) månader, HR 0.50; P<0.001.4
Varje år diagnostiseras cirka 1 300 nya fall av njurcancer i Sverige.

Vi har listat några appar som kan hjälpa dig i ditt dagliga arbete i sjukvården.

KEYTRUDA® (pembrolizumab) sex veckors-doseringsschema kan vara ett praktiskt val för både patienter och läkare
KEYTRUDA® (pembrolizumab); 25 mg/ml koncentrat till infusionsvätska, lösning. Antineoplastiska medel, PD-1/PDL-1-hämmare, L01FF02, Rx, Subventioneras ej, SPC 06/2024
Indikationer:
Melanom
Icke-småcellig lungcancer (NSCLC)
KEYTRUDA i kombination med platinabaserad kemoterapi som neoadjuvant behandling, och därefter fortsatt som monoterapi för adjuvant behandling, är indicerat för behandling av resektabel icke‑småcellig lungcancer hos vuxna med hög risk för recidiv.
KEYTRUDA som monoterapi är indicerat för behandling av vuxna patienter med:
KEYTRUDA som kombinationsbehandling är indicerat för vuxna patienter med:
Klassiskt Hodgkins lymfom (cHL)
Urotelial cancer (UC)
Skivepitelcancer i huvud och hals (HNSCC)
Njurcellscancer (RCC)
Cancer som uppvisar hög mikrosatellitinstabilitet (MSI-H) eller defekt mismatch repair (dMMR)
Kolorektalcancer (CRC)
KEYTRUDA som monoterapi är indicerat för vuxna med CRC som uppvisar MSI-H eller dMMR i följande behandlingslinjer:
Icke-kolorektal cancer
KEYTRUDA som monoterapi är indicerat för behandling av följande tumörer som uppvisar MSI-H eller dMMR hos vuxna med:
Esofaguscancer
Trippelnegativ bröstcancer (TNBC)
Endometriecancer (EC)
Cervixcancer
Adenokarcinom i ventrikel eller gastroesofageala övergången
Gallvägscancer
Dosering och administreringssätt: Behandling ska initieras och övervakas av specialistläkare med erfarenhet av cancerbehandling. Om PD-L1-uttrycket specificeras i indikationen ska patienturvalet för behandling med KEYTRUDA baseras på tumöruttrycket av PD-L1, vilket bekräftas med en validerad testmetod. Om specificerat i indikationen ska patienturvalet för behandling med KEYTRUDA baseras på tumörstatus avseende MSI-H/dMMR, vilket bör bekräftas med en validerad testmetod.
Den rekommenderade dosen av KEYTRUDA för vuxna är antingen 200 mg var 3:e vecka eller 400 mg var 6:e vecka administrerat som en intravenös infusion under 30 minuter.
Den rekommenderade dosen av KEYTRUDA som monoterapi för pediatriska patienter från 3 år med cHL eller för patienter från 12 års ålder med melanom är 2 mg/kg kroppsvikt (upp till maximal dos på 200 mg), var 3:e vecka administrerat som en intravenös infusion under 30 minuter.
Patienter bör behandlas med KEYTRUDA till dess att sjukdomsprogression eller oacceptabel toxicitet inträffar (och upp till maximal behandlingstid om det är specificerat för en indikation). Det rekommenderas att kliniskt stabila patienter med initialt tecken på sjukdomsprogression ska stå kvar på behandling till dess att sjukdomsprogress har bekräftats. För adjuvant behandling av melanom, NSCLC eller RCC ska KEYTRUDA administreras till och med sjukdomsrecidiv, oacceptabel toxicitet eller maximalt under ett års tid. För neoadjuvant och adjuvant behandling av TNBC ska patienter behandlas neoadjuvant i kombination med kemoterapi med 8 doser KEYTRUDA 200 mg var 3:e vecka eller 4 doser med 400 mg var 6:e vecka eller till sjukdomsprogression som omöjliggör komplett resektion eller oacceptabel toxicitet. Detta följs av adjuvant behandling med 9 doser KEYTRUDA 200 mg var 3:e vecka eller 5 doser KEYTRUDA 400 mg var 6:e vecka som monoterapi eller till recidiv eller oacceptabel toxicitet. Patienter med sjukdomsprogression som omöjliggör komplett resektion eller som får oacceptabel toxicitet relaterat till KEYTRUDA i kombination med kemoterapi vid neoadjuvant behandling ska inte få KEYTRUDA som monoterapi för adjuvant behandling.
Vid administrering av KEYTRUDA som en del av en kombinationsbehandling med intravenös kemoterapi ska KEYTRUDA administreras först. Se även förskrivningsinformationen för kemoterapierna och övriga läkemedel som administreras i kombination med KEYTRUDA.
Behandling med KEYTRUDA ska sättas ut permanent vid följande tillstånd:
Vid användning i kombination med lenvatinib ska ett eller båda läkemedlen avbrytas vid behov. Lenvatinib ska pausas, dosreduceras eller sättas ut i enlighet med förskrivningsinformationen för lenvatinib vid kombination med KEYTRUDA. Ingen dosreducering rekommenderas för KEYTRUDA.
Kontraindikationer: Överkänslighet mot den aktiva substansen eller mot något hjälpämne.
Varningar och försiktighet: För påvisande av tumörens PD-L1-uttryck är det viktigt att välja en validerad och robust metod för att minimera antalet falskt negativa eller falskt positiva utfall.
De flesta immunmedierade biverkningar som förekom under behandling med KEYTRUDA var reversibla och hanterades med uppehåll i behandlingen med KEYTRUDA, administrering av kortikosteroider och/eller understödjande behandling. Immunmedierade biverkningar har också debuterat efter den sista dosen av KEYTRUDA.
För biverkningar som misstänks vara immunmedierade bör lämplig utvärdering utföras för att bekräfta etiologin eller utesluta andra orsaker. För patienter vars immunmedierade biverkningar inte kunde kontrolleras med kortikosteroider kan, baserat på begränsade data från kliniska studier, andra systemiska immunsuppressiva läkemedel övervägas. Immunmedierade biverkningar som förekommit i samband med behandling inkluderar pneumonit, kolit, hepatit, nefrit och endokrinopatier.
Långvarig hormonell substitutionsbehandling kan vara nödvändig i fall av immunmedierade endokrinopatier. Allvarliga immunmedierade hudbiverkningar har rapporterats hos patienter som fått KEYTRUDA. Fall av SJS och TEN, vissa med dödlig utgång, har rapporterats hos patienter som fått KEYTRUDA. Om SJS eller TEN bekräftas ska KEYTRUDA sättas ut permanent. Ytterligare kliniskt signifikanta, immunmedierade biverkningar, inklusive allvarliga fall och fall med dödlig utgång, har rapporterats i kliniska studier eller efter godkännandet. Fall av graft-versus-host disease (GVHD) och hepatisk venös ocklusiv sjukdom (VOD) har observerats hos patienter med cHL som genomgått allogen hematopoetisk stamcellstransplantation (HSCT) efter tidigare exponering för KEYTRUDA.
Avstötning av organtransplantat har rapporterats efter godkännandet för försäljning hos patienter som behandlas med PD-1-hämmare. Behandling med KEYTRUDA kan öka avstötningsrisken hos organtransplanterade patienter.
Hos patienter som genomgått allogen HSCT har akut GVHD, inklusive GVHD med dödlig utgång, rapporterats efter behandling med KEYTRUDA. Till dess att ytterligare data blir tillgänglig, bör noggrant övervägande av de potentiella fördelarna med HSCT och den eventuella ökade risken för transplantationsrelaterade komplikationer göras från fall till fall.
Allvarliga infusionsrelaterade reaktioner, inklusive överkänslighetsreaktioner och anafylaxi, har rapporterats hos patienter som behandlats med KEYTRUDA.
KEYTRUDA i kombination med kemoterapi ska användas med försiktighet till patienter ≥ 75 år efter noggrant övervägande av det potentiella nytta-riskförhållandet på individuell basis. För användning av KEYTRUDA som adjuvant behandling av patienter med melanom har en trend mot ökad frekvens av svåra och allvarliga biverkningar hos patienter ≥ 75 år har observerats. Säkerhetsdata för KEYTRUDA som adjuvant behandling av patienter ≥ 75 år med melanom är begränsade.
Vid urotelial cancer ska läkaren innan insättning av behandling överväga den fördröjda effekten av KEYTRUDA hos patienter med sämre prognos som tidigare behandlats med platinabaserad kemoterapi. Vid användning av KEYTRUDA i kombinationsbehandling för patienter med NSCLC och HNSCC är de observerade biverkningsfrekvenserna högre, vilket speglar bidragen från var och en av komponenterna.
När KEYTRUDA ges med axitinib, har högre frekvenser än väntat rapporterats av förhöjda ALAT och ASAT av grad 3 och 4 hos patienter med avancerad RCC. Det saknas direkt jämförande studier av säkerheten för KEYTRUDA i kombinationsbehandling mot KEYTRUDA som monoterapi.
Kolangit och gallvägsrelaterade infektioner är inte ovanligt hos patienter med gallvägscancer. Patienter med gallvägscancer (speciellt de med stent i gallvägarna) ska därför undersökas för utveckling av kolangit eller gallvägsinfektion innan behandling påbörjas och regelbundet därefter.
Patientkort: Alla förskrivare av KEYTRUDA måste vara insatta i förskrivarformationen och behandlingsriktlinjerna avseende KEYTRUDA.
Förskrivaren måste diskutera riskerna med KEYTRUDA-behandling med patienten. Patienten ska förses med ett patientkort i samband med varje förskrivning.
Särskilda patientgrupper: Äldre; Ingen dosjustering behövs för patienter ≥ 65 år. Nedsatt njurfunktion; Ingen dosjustering behövs för patienter med lätt eller måttligt nedsatt njurfunktion. KEYTRUDA har inte studerats hos patienter med svårt nedsatt njurfunktion. Nedsatt leverfunktion; Ingen dosjustering behövs för patienter med lätt eller måttligt nedsatt leverfunktion. KEYTRUDA har inte studerats hos patienter med svårt nedsatt leverfunktion. Pediatrisk population; Säkerhet och effekt för KEYTRUDA för barn under 18 år har inte fastställts med undantag för pediatriska patienter med melanom eller cHL.
Biverkningar: KEYTRUDA förknippas oftast med immunmedierade biverkningar. De flesta av dessa, inklusive allvarliga biverkningar, gick i regress efter initiering av lämplig medicinsk behandling eller utsättande av KEYTRUDA. Säkerheten för KEYTRUDA som monoterapi har utvärderats hos 7 631 patienter med olika tumörtyper med avseende på fyra doser (2 mg/kg kroppsvikt var 3:e vecka, 200 mg var 3:e vecka eller 10 mg/kg kroppsvikt varannan eller var 3:e vecka) i kliniska studier. I denna patientgrupp var de vanligaste biverkningarna trötthet (31 %), diarré (22 %) och illamående (20 %). Majoriteten av de biverkningar som rapporterades var av grad 1 eller 2 i allvarlighetshetsgrad. De allvarligaste biverkningarna som rapporterades för monoterapi var immunmedierade biverkningar och allvarliga infusionsrelaterade reaktioner.
Säkerheten för KEYTRUDA i kombination med kemoterapi har utvärderats i kliniska studier omfattande 4787 patienter med olika tumörtyper som fick 200 mg, 2 mg/kg kroppsvikt eller 10 mg/kg kroppsvikt av KEYTRUDA var 3:e vecka. De mest frekvent förekommande biverkningarna var anemi (53 %), illamående (51 %), trötthet (35 %), diarré (34 %), , förstoppning (32 %), kräkningar (29 %), nedsatt aptit (28 %), neutropeni (28 %), sänkt antal neutrofiler (26 %) och alopeci (25 %). Incidensen av biverkningar av grad 3-5 hos patienter med NSCLC var 67 % för kombinationsbehandling med KEYTRUDA och 66 % för enbart kemoterapi, för patienter med HNSCC var incidensen 85 % för kombinationsbehandling med KEYTRUDA och 84 % för kemoterapi tillsammans med cetuximab. För patienter med esofaguscancer var incidensen 86 % för kombinationsbehandling med KEYTRUDA och 83 % för enbart kemoterapi, och för patienter med TNBC var incidensen 80 % för kombinationsbehandling med KEYTRUDA och 77 % för enbart kemoterapi. För patienter med cervixcancer var incidensen 82 % för kombinationsbehandling med pembrolizumab och 75 % för enbart kemoterapi, med eller utan bevacizumab, för patienter med ventrikelcancer var incidensen 75 % för kombinationsbehandling med pembrolizumab (kemoterapi med eller utan trastuzumab) och 79 % för kemoterapi med eller utan trastuzumab, och hos patienter med gallvägscancer var incidensen 85 % för kombinationsbehandling med pembrolizumab och 84 % för enbart kemoterapi.
Säkerheten för KEYTRUDA i kombination med axitinib eller lenvatinib vid avancerad RCC har utvärderats i kliniska studier med 1 456 patienter med avancerad RCC eller avancerad EC som fått 200 mg KEYTRUDA var 3:e vecka och antingen 5 mg axitinib två gånger dagligen eller 20 mg lenvatinib en gång dagligen, såsom lämpligt. I dessa patientpopulationer var de mest frekvent förekommande biverkningarna diarré (58 %), hypertoni (54 %), hypotyreos (46 %), trötthet (41 %), nedsatt aptit (40 %), illamående (40 %), artralgi (30 %), kräkningar (28 %), viktnedgång (28 %), dysfoni (28 %), buksmärta (28 %), proteinuri (27 %), palmar-plantar erytrodysestesi (26 %), hudutslag (26 %), stomatit (25 %), förstoppning (25 %), muskuloskeletal smärta (23 %), huvudvärk (23 %) och hosta (21 %). Incidensen av biverkningar grad 3-5 var 80 % för KEYTRUDA i kombination med antingen axitinib eller lenvatinib och 71 % för enbart sunitinib. För patienter med EC var incidensen av biverkningar grad 3-5 89 % för KEYTRUDA i kombination med lenvatinib och 73 % för enbart kemoterapi.
Följande mycket vanliga biverkningar rapporterades för ≥ 1 av 10 patienter:
Monoterapi: anemi, hypotyreos*, minskad aptit, huvudvärk, dyspné, hosta, diarré, buksmärta*, illamående, kräkning, förstoppning, hudutslag*, klåda*, muskuloskeletal smärta*, artralgi, trötthet, asteni, ödem*, pyrexi. Kombination med kemoterapi: anemi, neutropeni, trombocytopeni, hypotyreos*, hypokalemi, minskad aptit, sömnlöshet, perifer neuropati, huvudvärk, dyspné, hosta, diarré, kräkning, illamående, buksmärta*, förstoppning, alopeci, klåda*, hudutslag*, muskuloskeletal smärta*, artralgi, trötthet, asteni, pyrexi, , förhöjt ALAT/ASAT. Kombination med axitinib eller lenvatinib: infektion i urinvägarna,anemi, hypotyreos, minskad aptit, huvudvärk, förändrad smakuppfattning, hypertoni, dyspné, hosta, diarré, buksmärta*, illamående, kräkning, förstoppning, hudutslag*, klåda*, artralgi, muskuloskeletal smärta*, myosit*, smärta i extremiteter, trötthet, asteni, ödem*, pyrexi, förhöjt lipas, förhöjt ALAT/ASAT, förhöjt blodkreatinin.
Följande vanliga biverkningar rapporterades för 1-10 av 100 patienter:
Monoterapi: lunginflammation, trombocytopeni, neutropeni, lymfopeni, infusionsrelaterad reaktion*, hypertyreos, hyponatremi, hypokalemi, hypokalcemi, sömnlöshet, yrsel, perifer neuropati, letargi, förändrad smakuppfattning, torra ögon, hjärtarytmi inklusive förmaksflimmer, hypertoni, pneumonit*, kolit*, muntorrhet, hepatit*, allvarliga hudreaktioner*, hudrodnad, dermatit, torr hud, vitiligo*, eksem, alopeci, akneliknande utslag, smärta i extremiteter, myosit*, artrit*, influensaliknande symtom, frossa, förhöjt ASAT/ALAT, hyperkalcemi, förhöjda alkaliska fosfataser (ALP), förhöjd nivå av bilirubin i blodet, förhöjt blodkreatinin. Kombination med kemoterapi: lunginflammation, febril neutropeni, leukopeni, lymfopeni, infusionsrelaterad reaktion*, binjurebarksvikt*, tyreoidit*, hypertyreos*, hyponatremi, hypokalcemi, yrsel, förändrad smakuppfattning, letargi, torra ögon, hjärtarytmi inklusive förmaksflimmer, hypertoni, pneumonit*, kolit*, muntorrhet, gastrit, hepatit*, allvarliga hudreaktioner*, hudrodnad, dermatit, torr hud, akneliknande utslag, eksem, myosit*, smärta i extremiteter, artrit*, akut njurskada, ödem*, influensaliknande sjukdom, frossa, förhöjd nivå bilirubin i blodet, förhöjt alkaliskt fosfatas (ALP), förhöjt blodkreatinin, hyperkalcemi. Kombination med axitinib eller lenvatinib: lunginflammation, neutropeni, trombocytopeni, lymfopeni, leukopeni, infusionsrelaterad reaktion*, binjurebarksvikt*, hypertyreos, tyreoidit*, hyponatremi, hypokalemi, hypokalcemi, sömnlöshet, yrsel, perifer neuropati, letargi, torra ögon, hjärtarytmi inklusive förmaksflimmer, pneumonit*, kolit*, pankreatit*, gastrit, muntorrhet, hepatit*, allvarliga hudreaktioner*, dermatit, torr hud, hudrodnad, akneliknande utslag, alopeci, artrit*, nefrit*, influensaliknande sjukdom, frossa, förhöjt amylas, förhöjda ALP, hyperkalcemi, förhöjd nivå bilirubin i blodet.
*) Dessa termer representerar en grupp av relaterade händelser som beskriver ett medicinskt tillstånd snarare än en enstaka händelse.
Immunogenicitet: I kliniska studier med patienter som behandlades med KEYTRUDA 2 mg/kg kroppsvikt var 3:e vecka, 200 mg var 3:e vecka eller 10 mg/kg kroppsvikt varannan eller var 3:e vecka som monoterapi hade 36 (1,8 %) av 2 034 utvärderbara patienter positiva testsvar för behandlingsinducerade antikroppar mot KEYTRUDA, varav 9 (0,4%) patienter hade neutraliserande antikroppar mot KEYTRUDA. Det fanns inga tecken på förändrad farmakokinetisk profil eller säkerhetsprofil vid utveckling av anti- KEYTRUDA eller neutraliserande antikroppar.
Interaktioner: Inga formella farmakokinetiska interaktionsstudier har utförts med KEYTRUDA. Eftersom KEYTRUDA elimineras från cirkulationen genom katabolism förväntas inga metabola läkemedelsinteraktioner. Användning av systemiska kortikosteroider eller immunsuppressiva läkemedel före start av KEYTRUDA bör undvikas på grund av potentiell påverkan på KEYTRUDA:s farmakodynamiska aktivitet och effekt.
Fertilitet, graviditet och amning: Det finns inga data från användning av KEYTRUDA hos gravida kvinnor. KEYTRUDA ska inte användas under graviditet såvida inte kvinnans kliniska tillstånd kräver behandling med KEYTRUDA. Fertila kvinnor ska använda en effektiv preventivmetod under behandling med KEYTRUDA och under minst 4 månader efter den sista dosen av KEYTRUDA. Det är okänt om KEYTRUDA utsöndras i bröstmjölk. Ett beslut bör fattas om man ska avbryta amningen eller avbryta behandling med KEYTRUDA efter att man tagit hänsyn till fördelen med amning för barnet och fördelen med behandling för kvinnan. Inga kliniska data finns tillgängliga avseende eventuella effekter av KEYTRUDA på fertiliteten.
För fullständig information se fass.se
SE-KEY-00105 06/2024

För att se detta innehåll måste du vara kvalificerad sjukvårdspersonal. Arbetar du inom hälso- och sjukvården? Klicka för att bekräfta